
7 AML Treatments: Complete Guide to Acute Myeloid Leukemia Therapy
-
Comprendre la Leucémie Myéloïde Aiguë (AML)
-
L'Évolution des Traitements AML Depuis 2017
-
Les 7 Principaux AML Treatments Actuels
-
Venetoclax: Inhibiteur de BCL2 Révolutionnaire
-
Gemtuzumab Ozogamicin: Thérapie Ciblée CD33
-
Inhibiteurs de FLT3: Midostaurin
-
Gilteritinib et Quizartinib
-
Inhibiteurs d'IDH pour les Mutations IDH1 et IDH2
-
Agents Hypométhylants Combinés avec Venetoclax
-
Revumenib et Ziftomenib: Nouvelles Thérapies Ciblées
-
Stratégies de Traitement Selon l'Âge et les Comorbidités
-
Gestion des Effets Secondaires et Soins de Support
-
Conclusion: L'Avenir des Traitements de la Leucémie Myéloïde Aiguë

La leucémie myéloïde aiguë (AML) est un cancer du sang qui commence dans la moelle osseuse. Depuis 2017, les traitements pour l'AML ont beaucoup changé. De nouveaux agents thérapeutiques ont été approuvés.
Le traitement de cette maladie complexe connaît une révolution. Des thérapies ciblées visent des mutations génétiques spécifiques. Les inhibiteurs de FLT3 et d'IDH sont des avancées majeures. Ils changent radicalement les soins offerts aux patients.
Dans ce guide complet, nous allons explorer les sept traitements clés pour l'AML. Nous verrons les avancées récentes et leur impact sur les soins aux patients.
Points Clés à Retenir
● Nouveaux agents thérapeutiques approuvés depuis 2017
● Thérapies ciblées pour des mutations génétiques spécifiques
● Inhibiteurs de FLT3 et d'IDH
● Impact sur les soins prodigués aux patients
● Sept traitements clés pour l'AML
Comprendre la Leucémie Myéloïde Aiguë (AML)
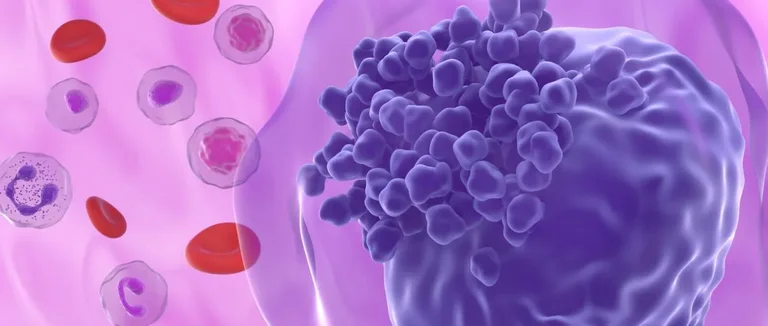
La leucémie myéloïde aiguë (AML) est un cancer grave de la moelle osseuse. Il faut bien la comprendre pour la traiter correctement. Cette maladie fait proliférer des cellules anormales dans la moelle, perturbant la production de cellules sanguines.
Définition et pathophysiologie
L'AML se caractérise par l'accumulation de cellules immatures dans la moelle et le sang. Cela vient d'une mauvaise régulation de la croissance cellulaire. Les altérations génétiques et moléculaires jouent un grand rôle dans cette maladie.
Les anomalies génétiques sont cruciales dans l'AML. Elles peuvent causer des mutations et des changements chromosomiques, affectant la croissance des cellules.
Épidémiologie et facteurs de risque
L'AML est plus fréquent chez les personnes âgées. Les facteurs de risque incluent l'exposition à des produits chimiques et à la radio. Les antécédents de troubles myéloprolifératifs augmentent aussi le risque.
| Facteur de risque | Description |
| Âge avancé | L'incidence de l'AML augmente avec l'âge |
| Exposition aux radiations | Les radiations ionisantes peuvent endommager l'ADN et provoquer des mutations |
| Exposition à des produits chimiques | Certains produits chimiques, comme le benzène, sont associés à un risque accru d'AML |
Symptômes et diagnostic
Les symptômes de l'AML incluent la fatigue et les infections récurrentes. On peut aussi avoir des saignements anormaux et des douleurs osseuses. Le diagnostic utilise des tests comme la NFS et l'examen de la moelle.
Un diagnostic précoce est crucial pour un traitement efficace. Les analyses cytogénétiques et moléculaires aident à identifier les anomalies génétiques.
En résumé, comprendre l'AML demande de connaître sa définition, sa pathophysiologie, son épidémiologie, les symptômes et le diagnostic. Cette connaissance est essentielle pour un traitement efficace.
L'Évolution des Traitements AML Depuis 2017
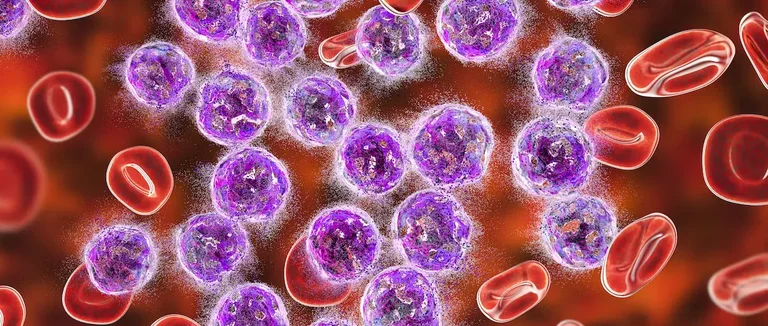
Les traitements contre l'AML ont beaucoup progressé depuis 2017. De nombreux nouveaux médicaments ont été approuvés aux États-Unis. Cette avancée a été due à des recherches et développements de thérapies ciblées.
Avancées majeures dans la recherche
Depuis 2017, 12 nouveaux agents ont été approuvés pour traiter l'AML aux États-Unis. Ces avancées sont cruciales pour les patients. On a vu l'apparition d'inhibiteurs de FLT3, d'inhibiteurs d'IDH, et de combinaisons d'agents hypométhylants avec des inhibiteurs de BCL2.
Ces nouvelles thérapies offrent des traitements plus personnalisés et efficaces. Les études ont montré des améliorations dans les taux de réponse et la survie globale.
Impact des nouveaux agents thérapeutiques
L'arrivée de ces nouveaux agents a changé le traitement de l'AML. Par exemple, les inhibiteurs de FLT3 ont amélioré les résultats pour les patients avec des mutations FLT3.
● Les inhibiteurs d'IDH (ivosidenib et enasidenib) ont montré leur efficacité chez les patients avec des mutations IDH1 et IDH2.
● Le venetoclax, un inhibiteur de BCL2, a été approuvé pour les patients âgés ou non aptes à la chimiothérapie intensive.
Amélioration des taux de survie
Les nouvelles thérapies ont grandement amélioré la survie des patients AML. Les données récentes montrent une amélioration de la survie globale, surtout chez les patients âgés et ceux avec des profils génétiques spécifiques.
Les efforts continuent pour améliorer les stratégies de traitement. La recherche explore de nouvelles combinaisons de thérapies et l'immunothérapie dans le traitement de l'AML.
Les 7 Principaux AML Treatments Actuels
Les traitements de la leucémie myéloïde aiguë (AML) ont beaucoup changé. Ils offrent de nouvelles chances aux patients. Nous allons voir les sept traitements principaux, leurs caractéristiques et comment ils sont utilisés.
Vue d'ensemble des options thérapeutiques
Les traitements pour l'AML incluent des innovations importantes. Parmi elles :
● Les inhibiteurs de FLT3
● Les inhibiteurs d'IDH
● Le Gemtuzumab Ozogamicin
● Les agents hypométhylants avec Venetoclax
● Revumenib et Ziftomenib
Ces traitements visent à répondre aux besoins de chaque patient. Ils tiennent compte de l'âge, des conditions de santé et des caractéristiques génétiques de la maladie.
Critères de sélection des traitements
Le choix du bon traitement pour l'AML repose sur plusieurs critères. Par exemple :
L'âge et l'état de santé du patient
Les caractéristiques de la leucémie
Les comorbidités
Les antécédents de traitement
Une analyse détaillée de ces critères aide à personnaliser le traitement. Cela augmente les chances de succès.
Importance de la médecine personnalisée
La médecine personnalisée est essentielle pour traiter l'AML. En adaptant les traitements aux besoins individuels, on améliore les résultats. On diminue aussi les effets secondaires.
La personnalisation des traitements permet de cibler les causes spécifiques de la maladie. Cela rend les traitements plus efficaces et mieux tolérés.
En résumé, les sept traitements AML actuels offrent des options innovantes et personnalisées. Le choix du traitement dépend d'une évaluation précise des caractéristiques du patient et de la maladie. Cela montre l'importance de la médecine personnalisée dans le traitement de l'AML.
Venetoclax: Inhibiteur de BCL2 Révolutionnaire
Venetoclax est un nouveau traitement pour l'AML. Il montre une grande efficacité, surtout quand il est utilisé avec d'autres médicaments. Cette nouvelle méthode change la façon de traiter cette maladie.
Mécanisme d'action moléculaire
Venetoclax bloque la protéine BCL2. Cette protéine aide les cellules leucémiques à ne pas mourir. En la bloquant, les cellules cancéreuses peuvent mourir comme elles devraient.
Mécanisme d'action de Venetoclax
| Action | Description |
| Inhibition de BCL2 | Bloque la protéine anti-apoptotique BCL2 |
| Restauration de l'apoptose | Permet l'élimination des cellules cancéreuses |
Efficacité clinique et indications
Les études montrent que venetoclax améliore la vie des patients atteints d'AML. Il est particulièrement utile pour les personnes âgées ou qui ne peuvent pas faire de chimiothérapie forte.
« L'association de venetoclax avec des agents hypométhylants représente une avancée majeure dans le traitement de l'AML, offrant de nouvelles options thérapeutiques pour les patients. »
Protocoles de traitement et dosage
Le dosage de venetoclax dépend du traitement et des médicaments associés. Il est important de suivre les doses recommandées pour bien traiter la maladie sans risquer de toxicité.
En conclusion, venetoclax est un grand pas en avant pour traiter l'AML. Il offre de nouvelles chances aux patients.
Gemtuzumab Ozogamicin: Thérapie Ciblée CD33
Gemtuzumab ozogamicin est un traitement innovant pour l'AML. Il cible l'antigène CD33 sur les cellules cancéreuses. C'est une avancée majeure dans le combat contre la leucémie myéloïde aiguë.
Fonctionnement du conjugué anticorps-médicament
Gemtuzumab ozogamicin attache l'antigène CD33 sur les cellules AML. Après, il libère une substance qui tue les cellules cancéreuses. Cette méthode ciblée protège les cellules saines.
Résultats des essais cliniques
Les essais cliniques ont prouvé que gemtuzumab ozogamicin améliore les résultats pour les patients AML. Il est particulièrement efficace chez ceux avec beaucoup d'antigène CD33.
| Étude | Population | Résultats |
| ALFA-0701 | Patients AML CD33+ | Amélioration de la survie globale |
| MyloFrance-1 | Patients AML réfractaires ou en rechute | Taux de réponse encourageants |
Populations de patients appropriées
Gemtuzumab ozogamicin est idéal pour les patients AML avec CD33. Il est souvent choisi pour ceux qui ne répondent pas bien au traitement. Les médecins vérifient la présence de CD33 pour décider si le traitement est approprié.
En conclusion, gemtuzumab ozogamicin est une option efficace pour les patients AML avec CD33. Il améliore les résultats cliniques et la qualité de vie des patients.
Inhibiteurs de FLT3: Midostaurin, Gilteritinib et Quizartinib
Les inhibiteurs de FLT3 sont une grande avancée dans le traitement de la leucémie myéloïde aiguë (AML). Ils sont essentiels pour les patients avec des mutations FLT3. Ces mutations sont très courantes dans l'AML et rendent le pronostic moins favorable.
Importance des mutations FLT3 dans l'AML
Les mutations FLT3 sont très fréquentes dans l'AML, touchant environ 30% des patients. Elles se divisent en deux types principaux : les duplications en tandem interne (ITD) et les mutations du domaine tyrosine kinase (TKD). Les mutations FLT3-ITD sont particulièrement dangereuses, augmentant le risque de rechute et diminuant la survie globale.
Face à ces mutations, la recherche de traitements ciblés a conduit au développement des inhibiteurs de FLT3. Les inhibiteurs de FLT3 ont amélioré les résultats pour les patients AML avec mutations FLT3, offrant une nouvelle option thérapeutique.
Comparaison des différents inhibiteurs
Plusieurs inhibiteurs de FLT3 sont disponibles ou en développement, comme le midostaurin, le gilteritinib et le quizartinib. Chacun a des caractéristiques et des effets différents.
● Midostaurin : Premier inhibiteur de FLT3 approuvé, utilisé avec la chimiothérapie standard pour les nouveaux patients AML avec mutation FLT3.
● Gilteritinib : Pour les patients en rechute ou réfractaires avec mutation FLT3, il a amélioré la survie globale en monothérapie.
● Quizartinib : Un inhibiteur de FLT3 de deuxième génération, en évaluation dans des essais cliniques pour les patients AML avec mutation FLT3.
Le choix de l'inhibiteur de FLT3 dépend de plusieurs facteurs. Cela inclut le stade de la maladie, les mutations spécifiques et les comorbidités du patient.
Stratégies d'utilisation en première ligne et en rechute
L'utilisation des inhibiteurs de FLT3 varie selon le stade de la maladie.
En première ligne, le midostaurin est souvent associé à la chimiothérapie. Pour les patients en rechute, le gilteritinib est une option validée.
Des études visent à combiner différents inhibiteurs de FLT3 avec d'autres traitements. Cela vise à améliorer les résultats pour les patients AML avec mutations FLT3.
En conclusion, les inhibiteurs de FLT3 ont changé le traitement de l'AML pour les patients avec mutations FLT3. Le choix de l'inhibiteur et la stratégie de traitement dépendent de plusieurs facteurs, comme le stade de la maladie et les caractéristiques génétiques de l'AML.
Inhibiteurs d'IDH pour les Mutations IDH1 et IDH2
Les inhibiteurs d'IDH, comme l'ivosidenib et l'enasidenib, ont changé le traitement de l'AML. Ils visent directement les mutations IDH1 et IDH2. Ces mutations sont trouvées dans 20% des cas d'AML et aident à la croissance des cellules leucémiques.
Rôle des mutations IDH dans la pathogenèse
Les mutations IDH1 et IDH2 changent le métabolisme des cellules. Elles produisent du 2-hydroxyglutarate (2-HG) au lieu de l'α-cétoglutarate. Cela perturbe la régulation épigénétique et la différenciation cellulaire, aidant à la maladie.
Des études ont montré que les patients AML avec ces mutations ont des traits uniques. Cela justifie un traitement spécifique.
Ivosidenib (IDH1) et Enasidenib (IDH2)
L'ivosidenib et l'enasidenib ciblent spécifiquement les mutations IDH1 et IDH2. Ils réduisent le 2-HG et encouragent la différenciation des cellules leucémiques.
L'ivosidenib est approuvé pour l'AML en rechute ou réfractaire avec mutation IDH1. L'enasidenib est pour les patients avec mutation IDH2.
| Caractéristiques | Ivosidenib | Enasidenib |
| Cible | IDH1 muté | IDH2 muté |
| Indications | AML en rechute ou réfractaire | AML en rechute ou réfractaire |
| Mécanisme d'action | Inhibition de l'IDH1 muté, réduction du 2-HG | Inhibition de l'IDH2 muté, réduction du 2-HG |
Résultats des essais cliniques
Les essais ont montré que l'ivosidenib et l'enasidenib aident contre l'AML avec mutations IDH1 et IDH2. Les taux de réponse varient entre 30% et 40%. Certains patients atteignent même une rémission complète.
« L'utilisation d'inhibiteurs d'IDH a transformé le traitement de l'AML avec mutations IDH1 et IDH2. Cela offre une nouvelle option de traitement ciblé. »
Les études soulignent l'importance de détecter tôt les mutations IDH pour un traitement efficace.
Agents Hypométhylants Combinés avec Venetoclax
La combinaison des agents hypométhylants avec le venetoclax offre de nouvelles chances aux patients d'AML. Cette approche a donné de bons résultats, surtout pour les personnes âgées et fragiles.
Mécanismes de synergie thérapeutique
Les agents hypométhylants, comme l'azacitidine et la décitabine, diminuent la méthylation de l'ADN. Cela active les gènes qui combattent le cancer et aide les cellules à se différencier. Le venetoclax, un bloqueur de BCL2, empêche cette protéine de protéger les cellules leucémiques, favorisant leur mort.
En combinant ces deux, on cible plusieurs voies importantes pour la survie du cancer. Les essais cliniques ont montré une efficacité remarquable de cette combinaison, avec des taux de réponse plus élevés que la chimiothérapie seule.
Azacitidine et décitabine: différences et similitudes
L'azacitidine et la décitabine sont deux agents hypométhylants utilisés contre l'AML. Ils agissent de la même façon mais ont des différences dans leur pharmacocinétique et leurs effets secondaires.
● L'azacitidine est injectée sous la peau ou dans une veine, tandis que la décitabine est injectée dans une veine.
● Les deux peuvent causer des effets secondaires comme la baisse des globules, les nausées et la fatigue.
Le choix entre azacitidine et décitabine dépend des besoins de chaque patient et des protocoles de traitement.
Bénéfices pour les patients âgés et fragiles
Les patients âgés et fragiles avec l'AML profitent beaucoup de cette combinaison. Cette méthode offre une alternative aux traitements chimio intensifs, souvent trop durs pour eux.
Les études montrent que cette combinaison améliore la survie et les taux de réponse chez ces patients. Leur tolérance est aussi acceptable.
En résumé, l'association d'agents hypométhylants et venetoclax est une avancée majeure contre l'AML, surtout pour les patients âgés et fragiles. Cette synergie offre de nouvelles perspectives pour améliorer la vie des patients.
Revumenib et Ziftomenib: Nouvelles Thérapies Ciblées
La recherche sur l'AML a conduit au développement de nouvelles thérapies. Le revumenib et le ziftomenib sont des espoirs pour les patients. Ils visent des cibles spécifiques dans le corps.
Revumenib: Inhibiteur de Ménine pour les Translocations KMT2A
Le revumenib cible les translocations KMT2A, une cause commune de l'AML. Il montre des promesses dans les essais cliniques.
Les patients avec ces translocations ont un mauvais pronostic. Le revumenib pourrait être une nouvelle option pour eux. Les premiers résultats sont encourageants et méritent plus de recherches.
Ziftomenib: Agent Prometteur pour les Mutations NP
Le ziftomenib vise les mutations NP dans l'AML. Il est une approche innovante pour améliorer les traitements.
Les mutations NP sont importantes dans l'AML. Le ziftomenib a donné des résultats prometteurs dans les études précliniques. Les essais cliniques en cours vont évaluer sa sécurité et son efficacité.
Résultats Préliminaires et Perspectives d'Avenir
Les premiers résultats du revumenib et du ziftomenib sont prometteurs. Ils offrent de nouvelles perspectives pour traiter l'AML. Ces thérapies ciblées pourraient améliorer la survie et la qualité de vie des patients.
Voici un tableau des caractéristiques clés de ces deux thérapies :
| Caractéristique | Revumenib | Ziftomenib |
| Cible moléculaire | Translocations KMT2A | Mutations NP |
| Mécanisme d'action | Inhibiteur de ménine | Agent ciblant les mutations NP |
| Stade de développement | Essais cliniques en cours | Essais cliniques en cours |
En résumé, le revumenib et le ziftomenib sont des avancées importantes pour l'AML. Leur développement montre l'importance de la recherche et de la médecine personnalisée pour améliorer les soins aux patients.
Stratégies de Traitement Selon l'Âge et les Comorbidités
Les patients AML ont des besoins différents selon leur âge et santé. Nous allons voir comment on traite ces cas.
Approches pour les patients jeunes et en bonne santé
Pour les jeunes et en bonne santé, l'objectif est de guérir. Les traitements peuvent être :
● Chimiothérapie intensive
● Thérapies ciblées
● Transplantation de cellules souches
Ces méthodes visent à guérir tout en réduisant les risques à long terme.
Adaptations pour les patients âgés (>75 ans)
Pour les plus de 75 ans, les traitements doivent être adaptés. Ils tiennent compte des comorbidités et fragilité. Les options incluent :
Thérapies à base d'agents hypométhylants
Venetoclax avec d'autres agents
Soins de support pour améliorer la qualité de vie
Il faut trouver un équilibre entre efficacité et tolérance pour ces patients.
Considérations pour les patients avec comorbidités significatives
Les patients avec comorbidités nécessitent une évaluation détaillée. On doit considérer :
● L'état cardiaque et rénal
● La présence de diabète ou d'autres conditions chroniques
● La capacité à tolérer les effets secondaires
Nous devons adapter les traitements pour réduire les risques et augmenter les bénéfices.
En conclusion, le traitement de l'AML doit être personnalisé. Il faut tenir compte de l'âge, des comorbidités et de l'état de santé. Cette approche améliore les résultats et la qualité de vie des patients.
Gestion des Effets Secondaires et Soins de Support
Les traitements AML peuvent changer la vie des patients. Il faut gérer les effets secondaires de façon proactive. Une approche globale des soins est cruciale pour réduire les effets négatifs et améliorer les résultats.
Effets secondaires communs à tous les traitements
Les patients AML peuvent avoir la fatigue, les nausées, les vomissements, la diarrhée et les infections. Ces problèmes viennent souvent de la myélosuppression, un effet des traitements anticancéreux.
La fatigue est un problème fréquent. Il affecte la vie quotidienne des patients. Pour la gérer, on peut conseiller de faire de l'exercice modéré et de bien gérer son énergie.
Toxicités spécifiques à chaque classe thérapeutique
Chaque type de traitement AML a ses propres effets secondaires. Par exemple, les inhibiteurs de FLT3 peuvent causer des diarrhées et des éruptions cutanées. Les agents hypométhylants peuvent causer des problèmes de sang.
Les inhibiteurs de BCL2 comme le vénétoclax peuvent causer des risques de lyse tumorale. Il faut surveiller de près et prendre des mesures préventives.
Stratégies préventives et interventions
La prévention et la gestion des effets secondaires nécessitent une approche multidisciplinaire. On utilise la prophylaxie anti-infectieuse, la gestion de la douleur, et les interventions nutritionnelles.
Des stratégies préventives comme l'utilisation de facteurs de croissance hématopoïétiques peuvent réduire les cytopénies et les risques d'infections.
"Une gestion proactive des effets secondaires est essentielle pour améliorer la qualité de vie des patients AML et optimiser les résultats thérapeutiques."
En conclusion, gérer les effets secondaires et offrir des soins de support sont essentiels pour les patients AML. Une approche personnalisée et proactive aide à réduire les effets négatifs et à améliorer les résultats.
Conclusion: L'Avenir des Traitements de la Leucémie Myéloïde Aiguë
Les traitements de la leucémie myéloïde aiguë (AML) connaissent des progrès importants. Cela offre de nouvelles chances aux patients et aux professionnels de la santé. Avec la recherche et les thérapies ciblées, l'avenir semble prometteur.
Nous avons vu les sept principaux traitements AML actuels. Parmi eux, les inhibiteurs de BCL2, les thérapies ciblées CD33, et les inhibiteurs de FLT3 et IDH. Ces avancées ont amélioré les chances de survie des patients.
La recherche continue est cruciale. Elle aide à développer de nouvelles thérapies et à améliorer les traitements. Ces efforts sont essentiels pour offrir les meilleurs soins aux patients. L'avenir des traitements AML promet donc de nouvelles options et une meilleure qualité de vie.
Foire Aux Questions
La leucémie myéloïde aiguë (AML) est un cancer du sang. Il se caractérise par une prolifération anormale de cellules myéloïdes dans la moelle osseuse.
Les symptômes de l'AML incluent la fatigue et les infections fréquentes. On peut aussi avoir des saignements ou des ecchymoses faciles. La douleur osseuse ou articulaire est également courante.
Pour diagnostiquer l'AML, on utilise plusieurs tests. On fait une numération globulaire complète et un frottis sanguin. Une biopsie de la moelle osseuse et des analyses cytogénétiques et moléculaires sont aussi nécessaires.
Les traitements pour l'AML incluent la chimiothérapie. On utilise aussi des thérapies ciblées comme les inhibiteurs de FLT3 et d'IDH. Les agents hypométhylants sont parfois utilisés. Dans certains cas, la greffe de cellules souches est une option.
Le venetoclax est un inhibiteur de BCL2. Il bloque la protéine BCL2. Cela permet aux cellules cancéreuses de mourir par apoptose.
Les effets secondaires incluent la neutropénie et la thrombocytopénie. On peut aussi avoir de l'anémie, des infections, des nausées et des vomissements. La fatigue est également fréquente.
Le choix du traitement AML dépend de plusieurs facteurs. On considère l'âge, les comorbidités, et les caractéristiques de la leucémie. La réponse aux traitements antérieurs est aussi prise en compte.
Les mutations FLT3 rendent l'AML plus agressif. Elles peuvent être ciblées par des inhibiteurs de FLT3 comme le midostaurin et le gilteritinib.
La médecine personnalisée adapte le traitement à chaque patient. Elle prend en compte les caractéristiques de la leucémie et du patient, comme les profils cytogénétiques et moléculaires.
La combinaison d'agents hypométhylants et de venetoclax améliore l'efficacité du traitement. Cela est particulièrement bénéfique pour les patients âgés et fragiles.
Les perspectives incluent le développement de nouvelles thérapies ciblées. On espère aussi améliorer les stratégies de combinaison. L'immunothérapie pourrait être intégrée dans le traitement de l'AML.
* Le contenu de notre site web est uniquement destiné à des fins d'information. Veuillez consulter votre médecin pour obtenir un diagnostic et un traitement. Le contenu de la page ne contient pas d'informations sur les services de santé thérapeutiques de l'hôpital Liv.













