
Как собираются стволовые клетки: этапы в Лив Хоспитал
-
Основные источники стволовых клеток
-
Методы получения костного мозга
-
Получение мезенхимальных стволовых клеток из жировой ткани
-
Сбор эмбриональных и плодных стволовых клеток
-
Подготовка и хранение собранных клеток для терапии
-
Почему стоит выбрать Лив Хоспитал
В современной медицине всё чаще задают вопрос, как собираются стволовые клетки для применения в регенеративных процедурах. Ответ на него важен как для пациентов, планирующих терапию, так и для специалистов, подбирающих оптимальный протокол. Стволовые клетки способны восстанавливать повреждённые ткани, ускорять заживление и даже лечить некоторые хронические заболевания.
Согласно последним исследованиям, ежегодно в мире собирают более 500 000 донорских образцов, из которых часть используется в клинических испытаниях, а часть – в коммерческих программах лечения. Однако процесс их получения остаётся малоизвестным широкому кругу людей, что порой приводит к недоверию и страху.
В этой статье мы подробно разберём, откуда берутся стволовые клетки, какие существуют методики их извлечения, как происходит их очистка и хранение, а также какие требования предъявляются к качеству материала. Вы получите полное представление о технологическом пути от донора до готовой к применению клеточной терапии.
Основные источники стволовых клеток
Первый шаг в любой клеточной терапии – определить, из какого биологического материала будет получен материал. На сегодняшний день выделяют четыре ключевых источника:
- Костный мозг – богатый гематопоэтическими стволовыми клетками (ГСК), которые способны дифференцировать в клетки крови.
- Пупочная кровь – содержит мезенхимальные стволовые клетки (МСК) и гемопоэтические клетки, легко доступные при родах.
- Жировая ткань – один из самых доступных источников МСК, получаемых через липосакцию.
- Эмбриональные и плодные клетки – получаемые из эмбрионов в рамках программ ЭКО, обладают плюрипотентностью.
Выбор источника зависит от цели терапии, возраста пациента и наличия донорского материала. Например, для лечения гемофилии предпочтительнее использовать костный мозг, а для регенерации хрящевой ткани – мезенхимальные клетки из жировой ткани.
| Источник | Тип клеток | Плюсы | Минусы |
|---|---|---|---|
| Костный мозг | ГСК, МСК | Высокая потенция, проверенный клинический опыт | Инвазивная процедура, требует анестезии |
| Пупочная кровь | ГСК, МСК | Минимальная инвазивность, богатый материал | Ограниченный объём, доступно только при родах |
| Жировая ткань | МСК | Большой объём, простота получения | Требует липосакции, возможные осложнения |
| Эмбриональные клетки | Плюрипотентные | Широкий спектр дифференциации | Этические вопросы, строгие регулятивные ограничения |

Методы получения костного мозга
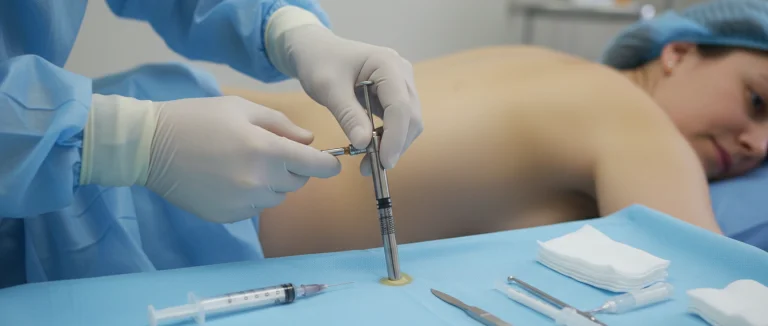
Костный мозг остаётся золотым стандартом для получения гемопоэтических стволовых клеток. Наиболее распространённый метод – аспирация костного мозга (BM aspiration). Процедура проходит под местной анестезией, обычно в области тазовой кости (остеальная кость). Специалист вводит специальную иглу, присоединённую к вакуумному шприцу, и извлекает небольшие объёмы костномозговой жидкости.
Этапы процедуры
- Подготовка пациента: анализы крови, оценка свертывающей системы.
- Обезболивание: местная анестезия или лёгкая седатация.
- Аспирация: ввод иглы, сбор 50–100 мл костномозговой жидкости.
- Обработка: центрифугирование для отделения клеточного слоя от плазмы.
- Контроль качества: подсчёт количества CD34+ клеток, проверка стерильности.
После извлечения материал проходит очистку с помощью автоматических сепараторов, которые позволяют получить концентрат клеток высокой чистоты. Важно отметить, что в процессе аспирации может возникнуть небольшое кровотечение, однако осложнения редки.
Для пациентов, которым требуется автологичная трансплантация (самостоятельный материал), процедура может повторяться несколько раз, чтобы собрать достаточный объём клеток. В случае аллогенной трансплантации (донорский материал) используется совместимый донор, а процесс сбора аналогичен.
Получение мезенхимальных стволовых клеток из жировой ткани
Жировая ткань (адипоз) стала популярным источником МСК благодаря своей доступности и относительно низкой инвазивности. Основной метод – липосакция, при которой удаляется небольшое количество подкожного жира, обычно из области живота или бедер.
Технологический процесс
- Липосакция: ввод канюли под кожей, отсос жировой ткани в стерильный контейнер.
- Обработка: ферментативное разрушение внеклеточного матрикса с помощью коллагеназы.
- Центрифугирование: отделение стромальных клеток от жирных капель.
- Культивирование: рост клеток в специализированных культуральных средах до нужного количества.
- Контроль качества: проверка морфологии, экспрессии маркеров CD73, CD90, CD105.
Полученные МСК могут быть использованы в регенеративных процедурах для восстановления хрящей, костей, сухожилий и даже кожи. Автологичный подход (когда материал берётся у самого пациента) минимизирует риск иммунных реакций.
Важно, что процесс культивирования происходит в условиях GMP (Good Manufacturing Practice), что гарантирует соответствие международным стандартам качества и безопасности.
Сбор эмбриональных и плодных стволовых клеток
Эмбриональные стволовые клетки (ЭСК) обладают плюрипотентностью, то есть способны дифференцировать в любой тип клеток организма. Их получение связано с программами экстракорпорального оплодотворения (ЭКО), когда излишки эмбрионов, не планируемых к имплантации, используют для научных и терапевтических целей.
Этапы получения
- ЭКО: оплодотворение яйцеклетки сперматозоидом in vitro.
- Культивирование эмбрионов до бластоцисты (5‑6 дней).
- Отбор избыточных эмбрионов с согласия доноров.
- Извлечение внутренней клеточной массы (ICM) и культивирование в специальных средах.
- Контроль качества: проверка генетической стабильности, отсутствие дифференцированных клеток.
ЭСК широко исследуются в рамках регенеративной медицины, однако их использование регулируется строгими этическими и законодательными нормами. В Турции, где находится Лив Хоспитал, такие процедуры проводятся только в лицензированных центрах с полным соблюдением международных протоколов.
Для пациентов, интересующихся терапией с использованием эмбриональных клеток, важно обсудить альтернативы, такие как индуцированные плюрипотентные стволовые клетки (iPSC), получаемые из собственных клеток пациента и обладающие схожими свойствами без этических ограничений.
Подготовка и хранение собранных клеток для терапии
После того как стволовые клетки успешно собраны, их необходимо подготовить к последующему применению. Этот этап включает очистку, концентрацию, проверку качества и криоконсервирование.
Ключевые процессы
- Очистка: удаление гемолитических и микробиологических примесей с помощью фильтрации и центрифугирования.
- Концентрация: использование автоматических сепараторов для получения высоко концентрированного клеточного продукта.
- Тестирование: подсчёт жизнеспособных клеток (viability), определение маркеров CD34, CD45, CD73 и др., проверка стерильности.
- Криоконсервирование: замораживание в контролируемой скорости с криопротекторами (например, DMSO) и хранение в жидком азоте при –196 °C.
- Размораживание и подготовка к введению: постепенное оттаивание, удаление криопротектора, повторная проверка качества перед инфузией.
Качество клеточного продукта напрямую влияет на эффективность терапии. Поэтому в Лив Хоспитал применяется система контроля качества, соответствующая требованиям JCI и международным стандартам GMP.
Для пациентов, выбирающих международные программы лечения, важным преимуществом является возможность транспортировки криоконсервированных клеток в специализированных биоконтейнерах, что обеспечивает сохранность материала даже при длительных перелетах.
Почему стоит выбрать Лив Хоспитал
Лив Хоспитал – это аккредитованная JCI сеть частных больниц в Стамбуле, специализирующаяся на комплексных программах терапии стволовыми клетками. Мы предлагаем современное оборудование, опытных специалистов и индивидуальный подход к каждому пациенту, включая полную поддержку иностранных пациентов: запись на приём, трансфер, услуги переводчика и помощь с размещением.
Наши лаборатории соответствуют требованиям GMP, а процесс получения и обработки стволовых клеток полностью согласован с международными протоколами, что гарантирует высочайшее качество и безопасность лечения.
Готовы начать путь к восстановлению здоровья с помощью стволовых клеток? Свяжитесь с нашими специалистами уже сегодня, чтобы получить персональную консультацию и подобрать оптимальную программу лечения.
Часто задаваемые вопросы
Процесс начинается с выбора источника: костный мозг – через аспирацию, пупочная кровь – сразу после родов, жировая ткань – через липосакцию, эмбриональные клетки – из избыточных эмбрионов ЭКО. Затем материал проходит очистку, центрифугирование и контроль качества, после чего клетки могут быть заморожены в жидком азоте для дальнейшего использования в терапии.
Костный мозг богат гемопоэтическими стволовыми клетками, пупочная кровь содержит мезенхимальные и гемопоэтические клетки, жировая ткань предоставляет мезенхимальные клетки через липосакцию, а эмбриональные клетки обладают плюрипотентностью и могут дифференцировать в любой тип клеток. Выбор зависит от клинической задачи, возраста пациента и этических ограничений.
Сначала пациент проходит предоперационные анализы и оценку свертывающей системы. Затем под местной анестезией врач вводит вакуумный шприц в область тазовой кости, извлекая костномозговую жидкость. Полученный материал центрифугируют, отделяя клеточный слой, после чего проводят подсчёт CD34+ клеток и проверку стерильности. При необходимости процедура может повторяться для получения достаточного объёма клеток.
Жировая ткань берётся методом липосакции из области живота или бедер. Затем ферментативно разрушают внеклеточный матрикс коллагеназой, после чего центрифугируют для отделения стромальных клеток. Клетки выращивают в специализированных средах до нужного количества и проверяют морфологию, а также экспрессию маркеров CD73, CD90 и CD105, гарантируя соответствие GMP.
После очистки и концентрации клетки смешивают с криопротектором, обычно DMSO, и замораживают в специальных криоконтейнерах, контролируя скорость охлаждения. Затем вазы помещаются в резервуары с жидким азотом при –196 °C, где они могут храниться годами без потери жизнеспособности. При необходимости проводится постепенное оттаивание, удаление криопротектора и повторный контроль качества перед инфузией.
* Содержимое нашего сайта предназначено только для информационных целей. Обязательно обратитесь к врачу для диагностики и лечения. В содержание страницы не включены элементы, содержащие информацию о терапевтических медицинских услугах в Лив Госпитале.












