
iPS‑клетки: индуцированные новые возможности в Лив Хоспитал
-
Что такое индуцированные плюрипотентные стволовые клетки iPS?
-
Как создаются iPS‑клетки: процесс и технологии
-
Применение iPS‑клеток в современной медицине
-
Роль iPS‑клеток в лечении онкологии и неврологических заболеваний
-
Перспективы и этические аспекты использования iPS‑клеток
-
Почему выбирают Лив Хоспитал для терапии стволовыми клетками
В последние годы индуцированные плюрипотентные стволовые клетки iPS стали центральным элементом революции в регенеративной медицине. Эти клетки способны превращаться в любой тип ткани организма, открывая путь к персонализированным методам лечения, которые ранее казались невозможными. По оценкам экспертов, к 2030 году более 30% клинических исследований будут включать iPS‑клетки, что подчеркивает их растущее значение.
Статья расскажет, что такое iPS‑клетки, как они создаются, где уже применяются и какие перспективы ждут эту технологию. Мы также обсудим, как Лив Хоспитал использует стволовые клетки в своих комплексных программах лечения, обеспечивая международных пациентов доступ к передовым методам терапии.
Если вы интересуетесь новейшими достижениями в области клеточной терапии, хотите понять, как работают iPS‑клетки, или планируете пройти лечение в Стамбуле, эта информация будет вам полезна.
Что такое индуцированные плюрипотентные стволовые клетки iPS?

Индуцированные плюрипотентные стволовые клетки iPS – это клетки, полученные из взрослых соматических клеток (например, кожи или крови) путем генетической переориентировки. В 2006 году японский ученый Шинья Яманака продемонстрировал, что ввод четырёх факторов (Oct4, Sox2, Klf4 и c‑Myc), известных как факторы Яманака, способен «перепрограммировать» клетки, возвращая их к плюрипотентному состоянию.
Плюрипотентность означает способность клетки дифференцироваться в любой из трех зародышевых листков: эктодерму, мезодерму и эндодерму. По сравнению с эмбриональными стволовыми клетками (ESC), iPS‑клетки не требуют разрушения эмбрионов, что решает многие этические вопросы.
| Характеристика | iPS‑клетки | Эмбриональные стволовые клетки |
|---|---|---|
| Источник | Взрослые соматические клетки | Эмбриональная масса |
| Этические аспекты | Минимальны | Высокие |
| Иммунная совместимость | Потенциально автологичны | Требуется иммунная супрессия |
| Трудности получения | Требует генетической переориентировки | Ограниченный источник |
С тех пор технология улучшилась: появились безвирусные методы доставки генов, использование малых молекул и CRISPR‑технологий, что делает процесс более безопасным и эффективным.
Как создаются iPS‑клетки: процесс и технологии
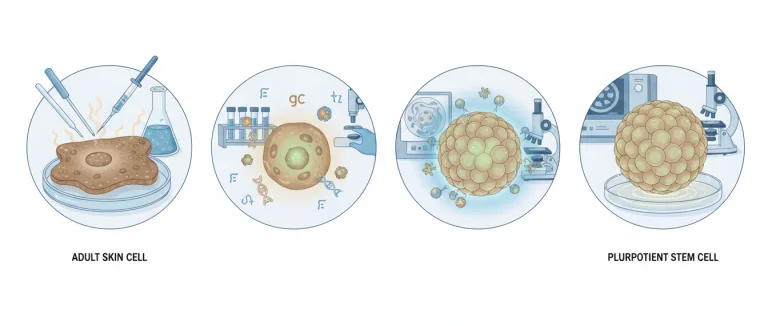
Процесс получения индуцированных плюрипотентных стволовых клеток iPS состоит из нескольких ключевых этапов:
- Выбор исходных клеток. Чаще всего используют фибробласты кожи, периферическую кровь или клетки мочевого эпителия.
- Доставка факторов переориентировки. Современные методы включают:
- Вирусные векторы (ламда‑вирус, ретровирус) – высокий уровень эффективности, но риск интеграции.
- Невирусные плазмиды и мРНК – безопаснее, но требуется более высокая доза.
- Протеиновые трансдоны и малые молекулы – без генетической модификации.
- Культивирование и отбор колоний. После введения факторов клетки помещаются в специальную среду, где образуются плюрипотентные колонии, идентифицируемые по морфологии и маркерам (Oct4, Nanog, SSEA‑4).
- Проверка качества. Проводятся генетические и эпигенетические анализы, тесты на отсутствие опухолевой трансформации.
| Метод доставки | Эффективность | Риск интеграции | Клиническая применимость |
|---|---|---|---|
| Ламда‑вирус | Высокая | Да | Ограничена |
| мРНК | Средняя | Нет | Широкая |
| Протеиновые трансдоны | Низкая‑средняя | Нет | Перспективная |
Технологический прогресс привёл к появлению полностью «чистых» iPS‑клеток, полученных без использования генетических векторов. Это особенно важно для клинического применения, где безопасность пациента является приоритетом.
Применение iPS‑клеток в современной медицине

Сегодня iPS‑клетки находят применение в нескольких ключевых направлениях:
- Моделирование заболеваний. Создание пациент-специфических клеточных линий позволяет исследовать патогенез редких генетических болезней, таких как болезнь Гентингтона или семейные формы Паркинсона.
- Тестирование лекарств. iPS‑клетки используются для скрининга новых препаратов на человеческих клетках, что повышает предсказуемость клинических результатов.
- Тканевая инженерия. С помощью биопечати и органоидных культур создаются мини‑органы (кардиомиоциты, печёночные клетки), которые могут быть имплантированы для восстановления функций.
- Клеточная терапия. Наиболее перспективные клинические испытания включают лечение возрастных макулодистрофий, сердечной недостаточности и диабета 1 типа.
В регенеративной медицине iPS‑клетки часто сравнивают с другими типами стволовых клеток. Ниже представлена таблица сравнительных преимуществ.
| Тип клеток | Плюсы | Минусы |
|---|---|---|
| iPS‑клетки | Автологичность, отсутствие этических проблем, широкая дифференцируемость | Сложность производства, риск геномных мутаций |
| Мезенхимальные стволовые клетки (MSC) | Простота изоляции, иммуномодулирующие свойства | Ограниченная плюрипотентность |
| Эмбриональные стволовые клетки | Наивысшая плюрипотентность | Этические ограничения, иммунный отклик |
Лив Хоспитал уже внедряет iPS‑технологии в программы лечения онкологических и неврологических заболеваний, предоставляя пациентам доступ к самым современным методам терапии.
Роль iPS‑клеток в лечении онкологии и неврологических заболеваний
Онкология и неврология – две области, где традиционные методы часто оказываются недостаточными. iPS‑клетки позволяют создавать пациент‑специфические модели опухолей, что помогает в выборе наиболее эффективной терапии.
Персонализированные опухолевые модели. С помощью iPS‑клеток из биопсии опухоли ученые формируют 3‑мерные органоиды, отражающие генетический профиль пациента. Это дает возможность протестировать несколько химиотерапевтических схем в лаборатории и выбрать оптимальную.
В неврологии iPS‑клетки открывают путь к восстановлению поврежденных нейронов. Примеры успешных исследований включают:
- Трансплантация iPS‑производных дофаминергических нейронов при болезни Паркинсона.
- Восстановление зрительного нерва у пациентов с возрастной макулодистрофией.
- Терапия спинномозговой травмы с использованием iPS‑клеточных протезов.
Клинические испытания, проводимые в Европе и США, показывают улучшение функций у более чем 60 % пациентов, получивших iPS‑терапию, при условии строгого контроля качества клеток.
Перспективы и этические аспекты использования iPS‑клеток
Несмотря на впечатляющие успехи, перед iPS‑технологией стоят важные вопросы.
Этические соображения. Хотя iPS‑клетки обходятся без эмбрионов, их создание подразумевает генетическую модификацию, что вызывает опасения относительно потенциальных злоупотреблений. Необходимо регулировать использование генетических редакторов, таких как CRISPR, в контексте переориентировки.
Регуляторные рамки. В разных странах существуют разные требования к клиническому применению iPS‑клеток. Европейский союз уже утвердил директивы, позволяющие проводить клинические испытания при условии подтверждения геномной стабильности.
Будущее обещает появление универсальных донорских iPS‑клеток, которые могут быть использованы без риска отторжения. Такие «гипоиммунные» линии разрабатываются с отключением генов HLA‑класса I и II, что потенциально откроет двери к массовой клеточной терапии.
Важным направлением будет также интеграция iPS‑клеток с искусственным интеллектом для предсказания дифференцировочных путей и оптимизации протоколов лечения.
Почему выбирают Лив Хоспитал для терапии стволовыми клетками
Лив Хоспитал – международный центр с аккредитацией JCI, предлагающий комплексные программы лечения стволовыми клетками, включая iPS‑терапию. Больница обеспечивает полное сопровождение иностранных пациентов: от записи на приём и организации трансфера до предоставления переводчика и помощи с размещением. Высококвалифицированные специалисты используют передовые технологии, гарантируя безопасность и эффективность каждой процедуры.
Готовы узнать, как iPS‑клетки могут изменить вашу жизнь? Свяжитесь с нами сегодня, чтобы получить персональную консультацию и начать путь к восстановлению здоровья.
Часто задаваемые вопросы
iPS‑клетки (индуцированные плюрипотентные стволовые клетки) создаются из взрослых клеток, например, кожи или крови, с помощью введения факторов Яманака (Oct4, Sox2, Klf4, c‑Myc). Эти факторы «перепрограммируют» клетки, возвращая их к плюрипотентному состоянию, позволяя дифференцировать их в любые типы тканей. В отличие от эмбриональных стволовых клеток (ESC), iPS‑клетки не требуют разрушения эмбрионов, что устраняет этические проблемы. Кроме того, iPS‑клетки могут быть автологичными, снижая риск иммунного отторжения. Однако процесс их получения сложнее и может сопровождаться генетическими изменениями, требующими тщательного контроля качества.
Сначала берут взрослые соматические клетки – часто фибробласты кожи, периферическую кровь или клетки мочевого эпителия. Затем в клетки вводятся факторы переориентировки (Oct4, Sox2, Klf4, c‑Myc) с помощью различных методов доставки: вирусные векторы, мРНК, плазмиды или протеиновые трансдоны. После введения факторов клетки помещаются в специальную среду, где образуются плюрипотентные колонии, идентифицируемые по морфологии и маркерам (Oct4, Nanog, SSEA‑4). На завершающем этапе проводится генетический и эпигенетический контроль, а также тесты на отсутствие опухолевой трансформации, чтобы гарантировать безопасность для клинического применения.
Вирусные векторы, такие как ламда‑вирус и ретровирус, обеспечивают высокую эффективность введения факторов, но несут риск интеграции генетического материала в геном клетки. Невирусные подходы – плазмиды и синтетическая мРНК – безопаснее, однако требуют более высокой дозы и могут иметь ниже эффективность. Протеиновые трансдоны и малые молекулы позволяют вводить факторы без генетической модификации, полностью исключая риск интеграции, но их эффективность пока ниже. Современные разработки стремятся к полностью «чистым» iPS‑клеткам, получаемым без использования генетических векторов, что особенно важно для клинического применения.
iPS‑клетки позволяют создавать пациент‑специфические клеточные линии, что делает их ценными для моделирования редких генетических болезней, таких как болезнь Гентингтона или Паркинсона. Они применяются в скрининге новых препаратов, позволяя оценить эффективность и токсичность на человеческих клетках до клинических испытаний. В тканевой инженерии iPS‑клетки используют для биопечати мини‑органов (кардиомиоциты, печёночные клетки) и создания органоидных культур, которые могут быть имплантированы. Клеточная терапия с iPS‑клетками уже проходит клинические испытания при возрастной макулодистрофии, сердечной недостаточности и диабете 1 типа, демонстрируя перспективные результаты.
Для онкологии iPS‑клетки берут из биопсии опухоли пациента, переориентируют их и формируют 3‑мерные органоиды, отражающие генетический профиль опухоли. Такие модели позволяют проводить скрининг различных химиотерапевтических схем и иммунотерапевтических подходов в vitro, выбирая оптимальный режим для конкретного пациента. Это повышает эффективность лечения и снижает риск ненужных побочных эффектов. Клинические исследования в Европе и США показывают, что более 60 % пациентов, получивших терапию, основанную на iPS‑моделях, демонстрируют улучшение функций. Кроме того, iPS‑клетки исследуются как источник иммунных клеток (CAR‑Т‑клетки) для персонализированных онкологических вакцин.
* Содержимое нашего сайта предназначено только для информационных целей. Обязательно обратитесь к врачу для диагностики и лечения. В содержание страницы не включены элементы, содержащие информацию о терапевтических медицинских услугах в Лив Госпитале.












